【技术突破】从细胞内到细胞表面:Src激酶定位重写50年教科书
1976年,我在查阅肿瘤学研究文献时,第一次遇到了Src这个名字。那时候的我还不知道,这个来自鸡肉瘤病毒的基因,会在此后半个世纪里反复出现在我的学术生涯中。
不可成药的经典癌基因
Src是第一个被鉴定的原癌基因,编码的c-Src激酶驱动超过50%的人类癌症发生。教科书告诉我们,这是一种严格的细胞内蛋白,通过N端豆蔻酰化修饰固定在细胞质膜内侧。所有试图从外部攻击它的精准武器——抗体药、CAR-T、ADC——都望"膜"兴叹。小分子抑制剂达沙替尼虽能进入细胞,但脱靶毒性和耐药问题始终无法解决。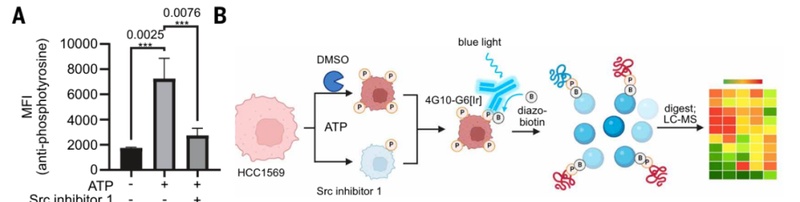
石破天惊的膜表面发现
2026年3月,加州大学旧金山分校JamesA.Wells教授团队采用光催化邻近标记技术,对癌细胞膜表面进行系统性蛋白普查。在738种细胞表面蛋白中,发现28种蛋白激酶,Src及其家族成员赫然在列。这是首次确凿证实Src可作为膜蛋白存在于癌细胞表面,研究人员将其命名为"eSrc"。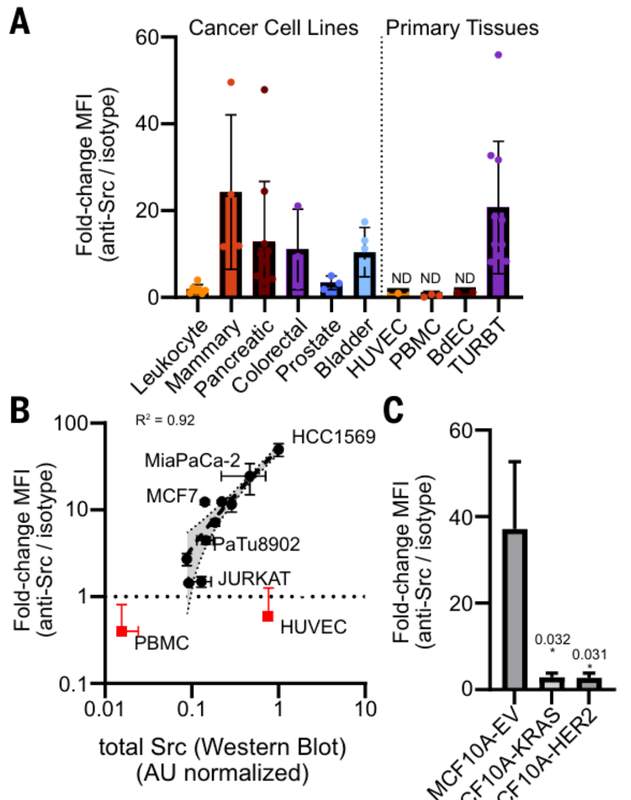
自噬溶酶体胞吐机制解析
eSrc如何突破膜屏障?CRISPR筛选、药物干预和活细胞成像锁定关键过程:自噬-溶酶体系统。癌细胞中异常活跃的自噬过程将Src"打包"进自噬体,随后自噬体与溶酶体融合形成自噬溶酶体。当自噬溶酶体与细胞膜融合进行胞吐时,膜结构翻转,原本朝内的Src结构域被完整暴露到细胞外。豆蔻酰化修饰是完成这场"旅行"的关键门票。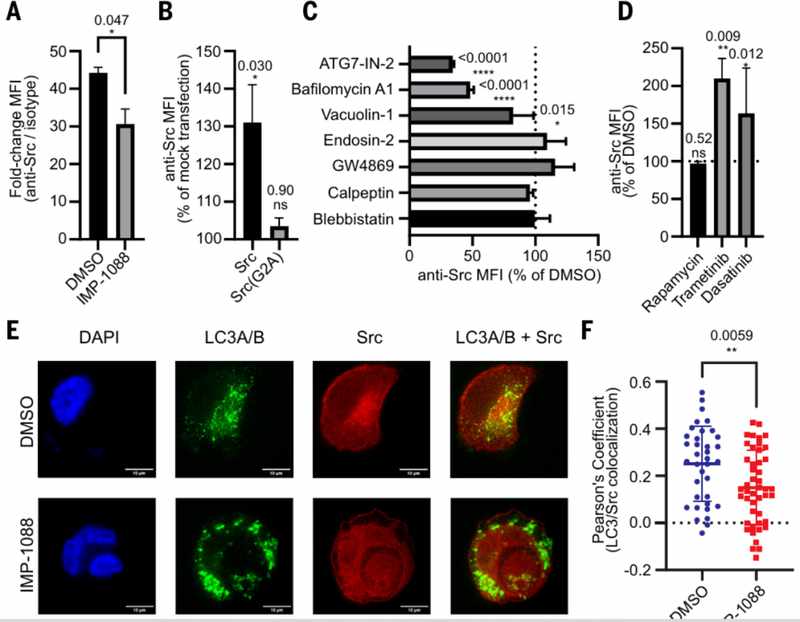
肿瘤特异性的精准验证
eSrc表达具有显著肿瘤特异性。永生化细胞系和癌细胞系中均能检测到eSrc,但健康供体来源的正常细胞中,即使细胞内Src表达量很高,表面也几乎检测不到eSrc。缺氧、营养匮乏等肿瘤微环境压力会显著上调自噬和溶酶体胞吐,促进eSrc表达。这意味着恶性程度越高、环境越恶劣的肿瘤,越容易暴露这个靶点。
精准靶向的全新纪元
针对eSrc开发的精准成像抗体偶联正电子核素,可在小鼠模型中清晰显示肿瘤位置。抗体与细胞毒素或放射性核素偶联构建的ADC或放射免疫偶联物,能显著抑制肿瘤生长且对正常组织毒性很低。eSrc还是T细胞衔接器双特异性抗体的理想靶点。这个曾经"不可成药"的癌基因,已成为可被精准打击的广谱抗癌靶点。
